На входе в кластер Бауманки «Инженерия в науках о жизни», где в научно-образовательном центре «Мягкая материя и физика флюидов» и на факультете биомедицинской техники работают ученые и инженеры, нас встретил его величество… нейрон. Это модель с двумя видами отростков – аксоном и дендритами – для эффективной коммуникации между клетками.
– С одной стороны нейрон, – это клетка – фундаментальная основа всего живого, – напоминает мне декан факультета и руководитель научно-образовательного центра, доктор физико-математических наук, главный научный сотрудник Станислав Юрченко. – А с другой – нейроны отвечают за первичную обработку информации, за работу самого загадочного органа нашего организма – мозга, за сознание, интеллект, чувства и даже гениальные открытия. Только представьте, что 1/5 всех усилий ученых в мире нацелена именно на понимание того, что такое мозг, как он себя «переизобретает», перестраивает, как развивается и стареет.
Как зарождается болезнь
Ученые объясняют: если вам повезет, то образование новых клеток и связей между ними в мозге сохранится на долгие годы, а если нет, – мозг с возрастом начнет увядать из-за накопления в нем множества лишнего «мусора». В случае развития болезни Паркинсона – это будет большое количество неправильного белка альфа-синуклеина, а в случае развития болезни Альцгеймера – бляшек из белка бета-амилоида.
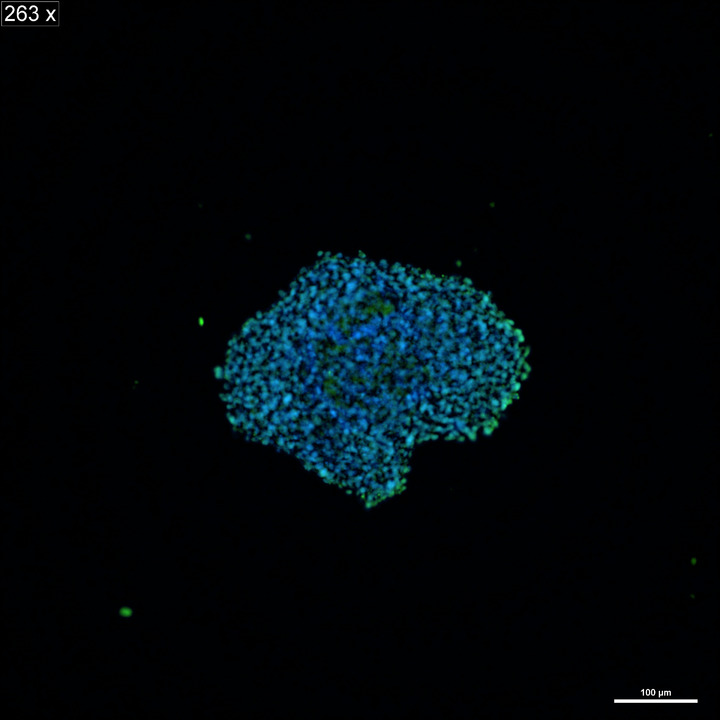
– У здорового человека в мозге присутствуют те же белки, но в правильной конформации и в физиологических концентрациях, – говорит главный научный сотрудник и заведующая лабораторией Научного центра неврологии, доктор медицинских наук, профессор Алла Салмина. – Они важны для взаимодействия клеток, пластичности мозга. И каждый из этих белков, если он оптимально выполняет свои функции, после должен быстро убираться из клеток и околоклеточного пространства, вовремя «дренироваться» тканевой жидкостью, что обычно происходит во время полноценного ночного сна.

Однако в случае наличия у таких белков дефектов, которые либо аномально изменяют их форму, либо препятствуют их удалению из тканей мозга, появляется риск их накопления, и это постепенно приводит к повреждению и гибели клеток, к снижению когнитивных функций человека.
Задача ученых, по словам Салминой, как раз заключается в том, чтобы как можно раньше находить именно такие, неправильно свернутые белки, и разрабатывать способы их восстановления или удаления.
Симптоматика может не проявляться очень долго, в течение 15-20 лет, но если есть генетическая предрасположенность к неврологическим заболеваниям или сыграли свою фатальную роль токсины, неправильный образ жизни и прочее, то где-то в мозге процесс накопления таких белков уже зарождается. Он протекает очень и очень медленно, и ученые всего мира нацелены сейчас на то, чтобы как можно раньше выявить его и подобрать для пациента правильный режим профилактики. Заметьте – еще не лечения!
Новый метод заглянуть в будущее
Один из новых методов, который разрабатывают сейчас неврологи, заключается в поиске неправильного белка в ликворе (цереброспинальной жидкости) или крови. Инициатором и руководителем проекта по разработке метода является директор Института мозга НЦН, академик РАН Сергей Иллариошкин.
По словам руководителя исследования, доктора медицинских наук Наталии Колотьевой, он называется методом индуцированной конверсии альфа-синуклеина в реальном времени.
– В какой-то мере он напоминает метод полимеразной цепной реакции (ПЦР), – говорит Наталия Александровна. – Поскольку другими лабораторными методами найти особый белок в самом начале зарождения болезни трудно (он находится в очень малой концентрации), то используют метод его амплификации – быстрого накопления – благодаря тому, что патологический белок запускает реакцию повреждения нормальных белков в пробирке. По мере накопления его можно регистрировать и делать вывод: есть у человека в организме неправильный белок или нет.
– Как же в идеале должен происходить такой поиск?
– За основу мы берем здоровые белки альфа-синуклеина, синтезированные искусственным образом. Потом к ним в пробирку, словно для затравки, добавляем образец жидкости пациента. Если запустится реакция, и со временем будет нарастать количество белков с неправильной формой, это значит, что есть что-то в жидкости донора, что запускает такую реакцию.
– Получается, что вы как бы моделируете в пробирке ту реакцию, которая приводит к накоплению патологических белков в ткани головного мозга?
– Да, но наша цель – за предельно короткое время получить эффективную агрегацию неправильных белков. Если они есть у человека, который про них еще не знает, наш метод проявит это. Неправильно свернутый белок может находиться в минимальных количествах, трудно определяемых другими методами, либо в ликворе, либо в крови.
– За рубежом работают над таким методом?
– Да, конечно, но на данном этапе никому еще не удалось его оптимизировать, чтобы использовать при скрининговых диагностических исследованиях. Минусы заключаются, во-первых, в том, что на такую диагностику потребуется несколько дней (чтобы получить количество патологических белков в пробирке, достаточное для определения), во-вторых, разработано много вариаций этого метода, но их воспроизводимость и чувствительность далеко не оптимальны, поэтому возможны и ложноположительные, и ложноотрицательные результаты.
– А что лучше подходит для выделения белка — ликвор или кровь?
– Пока мы работаем, в основном, с ликвором, но кровь удобнее для скрининга, поэтому, важно разработать протокол, который будет одинаково эффективен при работе с обоими видами биологических жидкостей.
– Насколько процесс в лаборатории проходит быстрее, чем в организме?
– В клетках образование патологических белков происходит за счет самых разных механизмов, и до сих пор вклад каждого из них в процесс накопления неправильно свернутых белков остается мало изученным. В пробирке патологический белок встречает сразу много мишеней и может с ними взаимодействовать, так мы в заведомо более простых условиях, чем в организме, пытаемся научиться регистрировать некоторые из механизмов развития нейродегенерации. Кстати, именно сотрудники МГТУ помогают нам ускорять реакцию.
– Как же вы ускоряете «возраст» белков в пробирке? – спрашиваю я Станислава Юрченко.
– Одно из направлений нашей работы – управляемая самосборка в мягкой материи, дизайн явлений в жидкостях при помощи внешних полей. Мы активно работаем над самыми различными режимами, воздействуя на коллоидные системы (физически и химически неоднородные смеси – Авт.) с белками электрическими и магнитными полями. В результате получается более эффективно запускать реакции каскадного взаимодействия патологических и нормальных белков in vitro (в пробирке – Авт.). В этом проекте удачно сочетаются компетенции биологов, врачей, биохимиков, физиков и инженеров – для того, чтобы создать удобный, высокочувствительный метод на новых физических принципах для диагностики нейродегенеративных заболеваний на самых ранних стадиях их развития.
Мозг на чипе
Во всем мире идет активное развитие другой перспективной технологии – создания «мозга-на-чипе». Это тоже тест-система, упрощенная модель мозга, на которой можно не только изучать развитие или старение мозга, механизмы развития заболеваний, но и оценивать действие новых препаратов против болезни Паркинсона, Альцгеймера и других заболеваний.
Идея объединить усилия специалистов разного профиля в таком проекте зародилась три года назад, и с 2022 года бауманцы и ученые НЦН работают в составе единого научного консорциума.
– Одной из наших целей стало воспроизведение на микрофлюидном чипе клеточных барьеров, которые ограничивают поступление лекарственных веществ из крови в ткань мозга и регулируют выведение из мозга метаболитов или белков, – говорит руководитель этого исследования Алла Салмина. – Это гематоэнцефалический барьер (стенка микрососудов – капилляров, пронизывающих ткань головного мозга) и гематоликворный барьер (клеточный слой, который ограничивает кровь от ликвора). Гематоликворный барьер изучен в меньшей степени, чем гематоэнцефалический, но его активность чрезвычайно важна для работы головного мозга. Поэтому мы задумали воспроизвести на чипе оба барьера, чего никто не делал раньше, «сложить» два вместе, как конструктор из кубиков, и таким образом сделать условия для тестирования лекарственных препаратов в таких системах более приближенными к естественным.

– На сегодняшний день мы создали несколько разных по архитектуре чипов, и поиск продолжается, в этой работе участвует сразу несколько научных центров МГТУ им. Баумана – «Мягкая материя и физика флюидов», «Функциональные микро/наноситемы». Кроме того, в нашей команде – химики, синтезирующие новые виды аналогов внеклеточного матрикса, физики, рассчитывающие оптимальные условия для заселения и оценки состояния клеток, клеточные биологи, работающие с культурами клеток, и специалисты многих других смежных направлений, – говорит Станислав Олегович.
– Что он вообще из себя представляет, этот мозг на чипе?
Ученый вместо долгого объяснения показывает мне маленькие прозрачные платформы из пластика, в которых есть маленькие каналы, камеры. В них подсаживают различные клетки, в том числе и те, что имитируют два барьера.
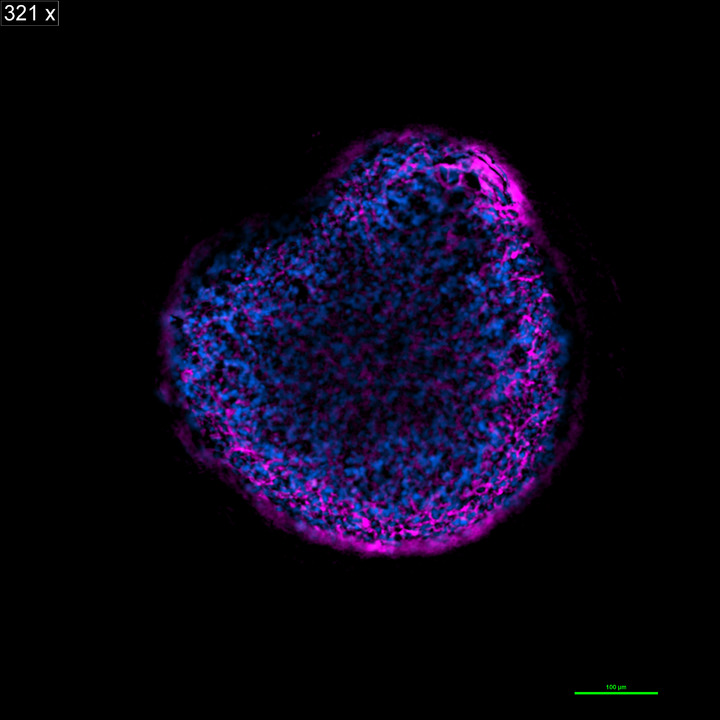
– Мозг на чипе дополняется у нас цифровой виртуальной моделью ткани головного мозга, – продолжает Юрченко. – На ней моделируется все процессы, к примеру, структурные, метаболические изменения клеток, движение тканевых жидкостей. Важно, что это область, где компетенции в области физики конденсированного состояния, физики мягкой материи и фазовых переходов необходимы для построения новых классов математических моделей. Другой пример – создание цифровых платформенных продуктов для анализа данных с применением технологий машинного обучения. Клеточные биологи обычно тратят много времени, к примеру, выявляя живые и неживые клетки, а мы сделали алгоритм, обучив нейросеть, благодаря которому эта работа ускоряется в несколько раз. Фактически, эти результаты должны кратно ускорить процесс клеточных исследований, помогая развивать передовые направления биомедицинской инженерии.
– Я еще слышала про работы с мини-мозгом. Что это такое?
– Это очень условное название – речь идет о церебральных органоидах (клеточные структуры – Авт.), которые можно получать in vitro из стволовых клеток, – объясняет Алла Борисовна. – Поэтому такие клеточные модели, в которых воспроизводятся, фактически, ранние этапы развития мозга, удобны для решения задач персонифицированной медицины. Кстати, и барьеры мозга на чипе можно получать с использованием клеток, специфичных для конкретного человека, – такие тест-системы ответят на вопрос, как лекарственный препарат проникает в ткань мозга данного пациента, и насколько эффективно он там работает.
– А степень проникновения через эти барьеры у каждого различна?
– Конечно! Кстати, добавлю, что у нас есть еще одно направление в работе с моделями мозга – мы изучаем на них процессы старения, естественные или ускоренные – при нейродегенерации. Те процессы, которые идут в организме десятки лет, в мозге-на-чипе или в органоиде проходят за считанные дни. Это хорошие современные модели для оценки индивидуальной траектории старения.
– Таким образом, у человека может быть двойник мозга в пробирке, при помощи которого он может представить, что ждет его впереди?
– Да, но это, конечно, не «двойник» мозга, а скорее упрощенная физическая модель некоторых его структурных модулей, например, взаимодействующих барьеров, в идеале дополненная математической моделью – «цифровым двойником», — дополняет Станислав Олегович.
И все-таки они восстанавливаются!
– По поводу того, восстанавливаются нервные клетки или нет, по-моему, есть еще разночтения. Так восстанавливаются или нет?
– Говорю вам абсолютно точно – восстанавливаются! – говорит Станислав Юрченко, — Но мы, конечно, не призываем к тому, чтобы их специально портить (улыбается).
– Они с нуля растут или каким-то образом производят самоомоложение?
– Есть область мозга, в которой происходит нейрогенез – рождение новых нервных клеток. Например, есть зоны в гиппокампе (височном отделе мозга – Авт.), где находятся стволовые клетки мозга. При получении внешних стимулов эти клетки начинают размножаться и дифференцироваться до нейронов или клеток глии (вспомогательных клеток нервной ткани – Авт.).
– Что за сигналы нужны для того, чтобы они пошли в рост?
– Разные, но как правило, они связаны с обучением, запоминанием, –добавляет Алла Салмина. – Поэтому для предотвращения старения мозга так важно получать и анализировать новую информацию, запоминать, расширять социальные контакты, приобретать новые навыки – учиться играть на музыкальных инструментах, вышивать, конструировать, но только до тех пор, пока этим мастерством вы не овладеете в совершенстве, и оно не перейдет в разряд рутинных.

Есть, кстати, другой, очень мощный стимул для рождения новых клеток мозга – его повреждение, когда сигналы из этой зоны начинают стимулировать нейрогенные ниши к генерации новых нейронов, которые должны не просто заполнить дефект ткани, но участвовать в обработке и передачи информации. К сожалению, такие механизмы очень ограничены, более того, ученые до сих пор дискутируют, насколько важен вклад нейрогенеза в восстановление головного мозга. Вместе с тем, отсюда становится понятной еще одна задача регенеративной неврологии – решить, что лучше: заставлять собственные стволовые клетки эффективно восстанавливаться или использовать трансплантированные?
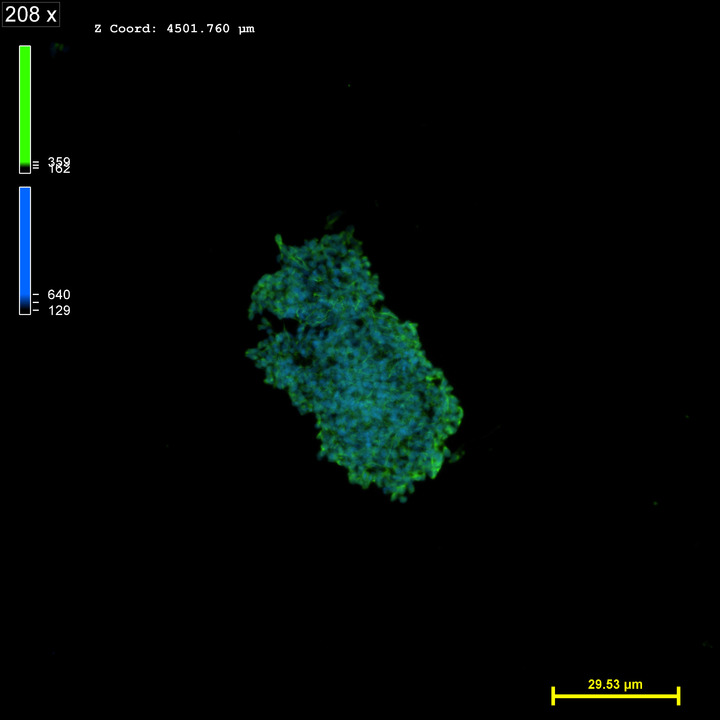
И еще один совет от команды нейробиологов, неврологов, биохимиков, физиков и инженеров: эффективная работа головного мозга напрямую зависит от полноценного сна. Важно спать положенное время – не менее 7-8 часов. Причем, засыпать надо вовремя, – в промежутке между 22 и 24 часами, когда в мозге идет выработка гормона сна – мелатонина, и именно во время сна активны механизмы очищения от патологически измененных белков и метаболитов, процессы нейрогенеза и восстановления поврежденных молекул и клеток.
Источник: mk.ru